आदर्श विलयन तथा अनादर्श विलयन में अंतर लिखे ideal and non ideal solution in hindi
(difference between ideal and non-ideal solution in hindi) आदर्श विलयन तथा अनादर्श विलयन में अंतर लिखे
| आदर्श विलयन (ideal solution) | अनादर्श विलयन (non-ideal solution) |
| 1. वे विलयन जो ताप तथा दाब की समस्त स्थिति पर राउल्ट के नियम की पालन करते है उन्हें आदर्श विलयन कहते है।
अर्थात P1 = P10 X1 P2 = P20 X2 P = P10 X1 + P20 X2 |
वे विलयन जो ताप तथा दाब की समस्त परास पर राउल्ट के नियम की पालन नहीं करते है उन्हें अनादर्श विलयन कहते है।
P1 ≠ P10 X1 P2 ≠ P20 X2 P ≠ P10 X1 + P20 X2 |
| 2. विलयन का कुल आयतन दोनों घटको के कुल आयतन के योग के बराबर होता है
अर्थात ΔVमिश्रण = 0 |
विलयन का कुल आयतन दोनों घटको के कुल आयतन के बराबर नहीं होता है।
अर्थात ΔVमिश्रण ≠ 0 |
| 3. विलेय तथा विलायक को मिलाने पर कोई उष्मीय परिवर्तन नहीं होते है।
अर्थात ΔHमिश्रण = 0 |
विलेय तथा विलायक को मिलाने पर कोई उष्मीय परिवर्तन होता है।
अर्थात ΔHमिश्रण ≠ 0 |
| 4. शुद्ध घटको के अणुओं के मध्य उतना ही आकर्षण होता है , जितना की विलयन के घटको के मध्य। | शुद्ध घटको के अणुओं के मध्य आकर्षण बल विलयन के अणुओं के मध्य लगने वाले आकर्षण बल से भिन्न होता है। |
| 5. उदाहरण :(1) हेक्सेन व हैप्टैन
(2) मैथिल अल्कोहल व एथिल अल्कोहल (3) क्लोरो बैंजीन व ब्रोमो बैंजीन
|
उदाहरण : (1) एथिल अल्कोहल व बेंजीन
(2) HNO3 + H2O (3) HCL + H2O (4) CO + क्लोरोफॉर्म |
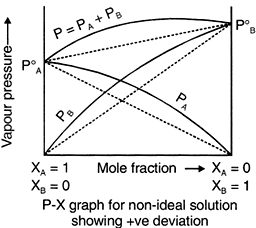
आदर्श विलयन के लिए वाष्पदाब तथा मोल अंश के मध्य ग्राफ
हिंदी माध्यम नोट्स
Class 6
Hindi social science science maths English
Class 7
Hindi social science science maths English
Class 8
Hindi social science science maths English
Class 9
Hindi social science science Maths English
Class 10
Hindi Social science science Maths English
Class 11
Hindi sociology physics physical education maths english economics geography History
chemistry business studies biology accountancy political science
Class 12
Hindi physics physical education maths english economics
chemistry business studies biology accountancy Political science History sociology
English medium Notes
Class 6
Hindi social science science maths English
Class 7
Hindi social science science maths English
Class 8
Hindi social science science maths English
Class 9
Hindi social science science Maths English
Class 10
Hindi Social science science Maths English
Class 11
Hindi physics physical education maths entrepreneurship english economics
chemistry business studies biology accountancy
Class 12
Hindi physics physical education maths entrepreneurship english economics
