hittorf method in hindi हिटॉर्फ विधि क्या है समझाइए हिटार्फ विधि के दोष लिखिए सचित्र
हिटॉर्फ विधि क्या है समझाइए हिटार्फ विधि के दोष लिखिए सचित्र hittorf method in hindi ?
अभिगमनांकों का प्रायोगिक निर्धारण (Experimental Determination of Transport Number) अभिगमनांकों के निर्धारण के लिए निम्न में से कोई एक विधि काम में लेते हैं-
(i) हिर्टाफ विधि (Hittroff Method)
(ii) चल सीमा विधि (Moving Boundary Method)
हिटार्फ विधि – यह विधि विद्युत अपघटन का प्रयोग करते समय ऐनोड़ तथा कैथोड कक्षों में सान्द्रता परिवर्तनों के अध्ययन पर निर्भर करती है।
सिद्धान्तः- जैसा कि उपरोक्त विवरण से स्पष्ट है कि किसी भी इलेक्ट्रोड विभाग में विद्युत अपघटयों की सान्द्रता में कमी उस आयन के चाल की समानुपाती होती है जो उस विभाग को छोड़कर जाते है
यदि सान्द्रता को ग्राम तुल्यांक में प्रदर्शित करें तो
चूंकि दोनों विभागों से विद्युत अपघट्य के ग्राम तुल्याकों में कमी प्रत्येक इलेक्ट्रोड़ पर जमा हुए ग्राम तुल्यांकों की संख्या के बराबर है अतः समीकरण (91) को निम्न प्रकार लिख सकते हैं।
प्रायोगिक विलयन के साथ परिपथ की श्रेणी में सिल्वर या कॉपर कूलॉमीटर लगाकर प्रत्येक इलेक्ट्रोड पर निक्षेपित तुल्यांकों की संख्या ज्ञात की जा सकती है प्रत्येक इलेक्ट्रोड पर निक्षेपित ग्राम तुल्यांक कूलामीटर के कैथोड पर निक्षेपित धातु के ग्राम तुल्यांको के बराबर होते हैं। अतः कैथोड़ पर जमा हुआ सिल्वर या कॉपर का भार ज्ञात कर लेते है। अतः समीकरण (92) को निम्न रूप से लिखा जा सकता है-
अतः हिटार्फ विधि द्वारा अभिगमनांक ज्ञात करने के लिए कैथोड़ या ऐनोड विभाग के ग्राम तुल्यांको की संख्या में कमी और कूलॉमीटर में निक्षेपित धातु के ग्राम तुल्यांको की संख्या को ज्ञात करना आवश्यक है ।
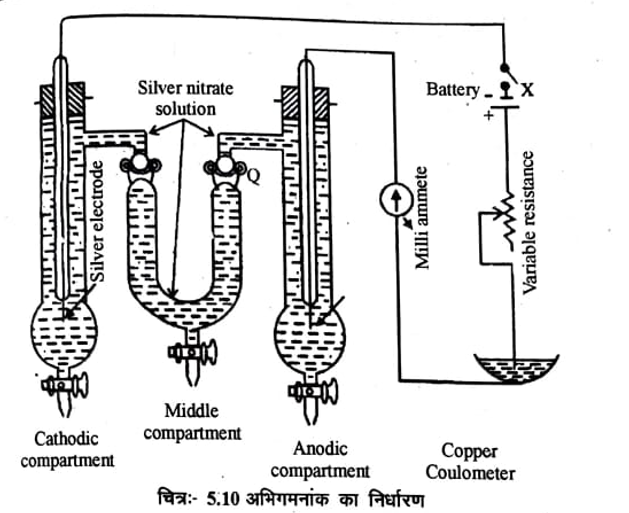
उपकरणः- अभिगमनांकों का निर्धारण हिटार्फ विधि द्वारा किया जाता है। हिटार्फ उपकरण का सामान्य रूप चित्र 5. ) में दिखाया गया है। इसमें दो ऊर्ध्वाकार नलियाँ A व B होती है जो बीच में एक U नली द्वारा परस्पर जुड़ी रहती है। नली A कैथोड़ नली B ऐनोंड कक्षों को तथा U नली मध्य कक्ष को प्रदर्शित करती है। तीनों नलियों के नीचे रोधनी टोटीयाँ (Stop cock) लगी होती है। U नली के सिरों पर भी P तथा Q रोधनी टोटीयाँ लगी रहती है जिसे बन्द करके कैथोड़ व ऐनोड नलियों के बीच आवागमन को बन्द किया जा सकता है। सम्पूर्ण उपकरण में ज्ञात सान्द्रता के विद्युत अपघट्य का विलयन भर देते हैं।
उपयुक्त धातु के इलेक्ट्रोड (जैसे सिल्वर, प्लेटिनम आदि) चित्र में दिखाए अनुसार A व B नलियों में फिट कर दिए जाते हैं। इन इलेक्ट्रोडों को मिली एमीटर M, कूलॉमीटर C, परिवर्ती प्रतिरोध R और बैटरी X से श्रेणी (Series) में जोड़ देते हैं। तत्पश्चात् 0.01 से 0.02 ऐम्पियर (10 से 20 मिली ऐम्पियर) की विद्युत धारा 2-3 घण्टे तक प्रवाहित की जाती है। जिससे कि दोनों कक्षों में विद्युत अपघट्य की सान्दता में इतना परिवर्तन हो जावे कि इसे मापा जा सके। परन्तु बहुत अधिक परिवर्तन नहीं होना चाहिए। प्रयोग के अन्त में U नली की रोधनियाँ P तथा Q को बन्द कर दिया जाता है ताकि दोनों कक्षों के विलयन एक दूसरे से नहीं मिल सके। शुष्क और तुले हुए अलग-अलग फ्लास्कों में तीनों विभागों से सम्पूर्ण विलयन निकाल कर उनका विश्लेषण कर लिया जाता है। मध्य विभाग के विलयन की सान्द्रता में परिवर्तन नहीं होना चाहिए। यदि इसमें परिवर्तन हो गया तो इसका मतलब यह है कि अधिक विद्युत धारा प्रवाहित हुई हैं। ऐसी परिस्थिती में प्रयोग फिर से दुबारा करना चाहिए। विश्लेषण में कमी का पता लगाया जाता है। कूलॉमीटर या वोल्टामीटर में निक्षेपित धातु की मात्रा भी ज्ञात करली जाती है। इलेक्ट्रोड की भिन्न-भिन्न प्रकृति के फलस्वरूप अनेक परिस्थितियाँ उत्पन्न हो जाती है। तीन ऐसी संभव स्थितियों के लिए अभिगमनांक निकालने के लिए सूत्रों का निगमन करेगें ।
(i) यदि वैद्युत अपघटन में इलेक्ट्रोड अप्रभावित रहते हैं:- इस विधि में प्लेटिनम या गोल्ड इलेक्ट्रोडों के बीच सिल्वर नाइट्रेट विलयन का वैद्युत अपघटन किया जाता है। इसमें वैद्युत अपघटन से प्राप्त उत्पाद (Ag’ या NO3) द्वारा इलेक्ट्रोड अप्रभावित रहती है। अतः अभिगमनांक की गणना सरल है।
गणनाः- माना कि वैद्युत अपघटन के पश्चात् x ग्राम एनोड विलयन में y ग्राम सिल्वर नाइट्रेट विलेय है तथा सिल्वर कॅलामीटर या वाल्टमीटर से W ग्राम सिल्वर निक्षेपित होती है।
II जब इलेक्ट्रोड विद्युत अपघटन के किसी एक उत्पाद से अभिक्रिया करते हैं:- मान लीजिए कि सिल्वर इलेक्ट्रोड़ के बीच सिल्वर नाइट्रेट विलयन का विद्युत अपघटन कराया जाता है। इस प्रयोग में Ag+ आयन के ऐनोड़ से कैथोड की ओर गमन के कारण एनोड के निकट इस विलयन में सिल्वर नाइट्रेट की सान्द्रता में वृद्धि पाई जाती है। इसका कारण यह है कि कैथोड से आने वाले नाइट्रेट (NO 3 ) आयन ऐनोड़ पर अनावेशित होकर सिल्वर इलेक्ट्रोड से क्रिया करके सिल्वर नाइट्रेट बनाते है जिससे ऐनोड कक्ष के विलयन में सिल्वर नाइट्रेट की सान्द्रता में वृद्धि हो जाती है।
माना कि प्रयोग में सिल्वर वोल्टामीटर में कैथोड़ पर W ग्राम सिल्वर निक्षेपित हुई। अतः फैराडे के नियानुसार सिल्वर इलेक्ट्रोड (ऐनोड) से W ग्राम सिल्वर घुल जायेगी और ऐनोड विलयन में मिल जायेगी । अर्थात ऐनोड़ कक्ष में सिल्वर की वृद्धि W ग्राम होनी चाहिए। माना कि प्रयोग के पश्चात् x ग्राम ऐनोड़ विलयन में y ग्राम सिल्वर नाइट्रेट है। अतः जल का भार = (x -y) ग्राम होगा। माना कि प्रयोग के प्रारम्भ में (x-y) ग्राम जल में z ग्राम सिल्वर नाइट्रेट था ।
यदि ऐनोड़ से चांदी के आयनों का अभिगमन न हुआ होता तो वृद्धि = W ग्राम होती लेकिन वास्तविक = w ग्राम होती है।
अतः सिल्वर आयनों (Ag+) के (ऐनोड विभाग से कैथोड विभाग की तरफ) अभिगमन के फलस्वरूप ऐनोड़ के चारों ओर सान्द्रण में कमी
जब विसर्जित आयन विलायक से क्रिया करते हैं:- जब प्लेटिनम इलेक्ट्रोड के बीच सोडियम हाइड्रक्साइड विलयन का विद्युत अपघटन करते है तो Na+ का कैथोड की ओर अभिगमन होता है। जहाँ ये आयन (Na+) अपना आवेश उदासीन कर जल से क्रिया करके NaOH बनाते हैं। अतः यदि कैथोड विलयन में NaOH के प्रारम्भिक और अन्तिम भारों को ज्ञात कर कैथोड़ के चारों ओर सान्द्रण में आभासी वृद्धि को ज्ञात कर सकते हैं। वास्तविक वृद्धि की गणना वोल्टामीटर को श्रेणी में लगाकर उसकी सहायता से की जा सकती है। Na+ और OH- के अभिगमनांकों की गणना स्थिति II के अनुसार करते हैं
हिटार्फ विधि के दोष – यद्यपि हिटार्फ विधि अभिगमनांकों के निर्धारण की एक सरल विधि है फिर भी इसमें कई दोष है:-
(1) इसमें विद्युत की बहुत कम धारा ( 10-20 मिली ऐम्पियर) प्रवाहित करते है जिससे विद्युत अपघटन बहुत धीरे होता है अतः इस विधि में समय अधिक लगता है ।
(2) विद्युत अपघटन के कारण विद्युत अपघट्य की सान्द्रता में थोड़ा परिवर्तन हो जाता है जिससे प्राप्त अभिगमनांकों के मान विद्युत अपघट्य की किसी निश्चित सान्द्रता के लिए नहीं होते ।
(3) विसरण व संवहन के कारण विलयन कुछ मात्रा में तो आपस में मिल ही जाते है। अतः यथार्थ परिणाम प्राप्त नहीं होते हैं
अतः अभिगमनांकों के निर्धारण के लिए एक अधिक सरल व यथार्थ विधि काम में लेते है जिसे चल सीमा पद्धति कहते हैं। हालांकि इसमें भी समय लगता है तथा सान्द्रता में परिवर्तन होता है परन्तु हिटार्फ विधि से सरल है यथार्थ परिणाम देती है।
चल सीमा विधि (Moving Boundary Method) :- इस विधि को लोज (Ledge) ने प्रतिपादित किया तथा बैंथम (Whenthm) ने सुधारा। इसके द्वारा लगाए गये विद्यत क्षेत्र के प्रभाव से आयनों की गति द्वारा सीधे ही अभिगमनांकों को निर्धारित करते हैं। यह विधि दो आयनिक विलयनों के बीच की सीमा के अभिगमन द्वारा आयनों की गतियों के अध्ययन पर निर्भर करती है।
सिद्धान्तः- इस विधि के सिद्धान्त को समझने के लिये धनायन के अभिगमनांक का निर्धारण करने का एक विशेष उदाहरण लेते है जैसे HCI विलयन मुख्य विद्युत अपघट्य (Main electerolyte) कहलाता है। इस कार्य के लिये एक दूसरे विद्युत अपघट्य का विलयन लेते है जिसे सूचक विद्युत अपघट्य (Indicator Electrolyte) कहते हैं। सूचक विद्युत अपघट्य के चयन में दो बातों का विशेष ध् यान रखा जाता है-
(1) सूचक विद्युत अपघट्य के धनायन का वेग, मुख्य विद्युत अपघट्य के धनायन से कम हो।
(2) मुख्य तथा सूचक विद्युत अपघट्य के ऋणायन समान (Common) हों ।
इसके अनुसार सूचक विद्युत अपघट्य CdCl2 लेते हैं जिसमे Ca2+ की चाल H’ से कम है तथा दोनों मे CI- आयन समान है।
उपकरण :- इस विधि में प्रयुक्त उपकरण चित्र 5.11 में दर्शाया गया है इसमें एक विद्युत अपघटनी सैल होता है, जिसका मध्य भाग समान व्यास वाली नली AB जैसा होता है। जिसे ऊर्वाकार स्थिति में लगा दिया जाता है। चित्र में दिखाये गये अनुसार इस नली में HCl तथा CdCl2 विलयन भरे जाते हैं। जिससे बीच वाली नली में दोनों विलयनों के बीच एक स्पष्ट सीमा aa’ दिखाई देती है। यदि विलयन रंगीन हो तो यह सीमा स्वतः ही स्पष्ट दिखाई देती है। अन्यथा रंगहीन विलयनों में CaCl2 विलयन की सान्द्रता ऐसी होनी चाहिये कि इसका घनत्व HCI विलयन के घनत्व से अधिक हो ताकि CaCl2 विलयन HCl विलयन से नीचे रहे तथा सीमा aa’ दोनों विलयनों के भिन्न-भिन्न अपर्वतनांकों के कारण देखी जा | HCl तथा CACI2 विलयनों में क्रमशः प्लेटिनम के तार को कैथोड नली के सिरे पर (HCI में) एवं कैडमियम छड़ को ऐनोड़ नली के पेन्दे पर CdCl2 के विलयन में लगा दिया जाता है।
बैटरी, परिवर्तनशील प्रतिरोध, ऐमीटर तथा कूलॉमीटर जो श्रेणी सम्बद्ध होते हैं के माध्यम से दोनों इलेक्ट्रोड़ों को चित्र में बताये अनुसार जोड़ दिया जाता है।
जब विद्युत धारा प्रवाहित की जाती है। तब H’ और Cd2+ आयन ऊपर कैथोड़ की तरफ चलते हैं तथा CI- आयन ऐनोड की तरफ नीचे चलते हैं चूंकि धीमी गति वाले Cd2+ आयन तेज गति वाले _H+ आयनों तक कभी नहीं पहुंच सकते अतः दोनों विलयनों के बीच तीक्ष्ण सीमा बनी रहती है। (Cd2+ आयन की गति H’ से कम है। यदि कम नहीं होगी तो विद्युत प्रवाहित करने पर सीमा अस्पष्ट हो जायेगी) प्रवाहित की गई विद्युत की मात्रा और सीमा द्वारा हटाने गये ( swept) आयन को जानते हुए अभिगमनांक सूत्र निकाला जा सकता है जो निम्नानुसार है-
गणना-माना कि विद्युत धारा कि एक निश्चित मात्रा प्रवाहित करने पर सीमा aa’ से bb’ पर आ जाती है। कैथेटोमीटर (Cathetometer) की सहायता से इस सीमा का विस्थापन (aa’ से bb) सही सही माप लिया जाता है। माना कि यह विस्थापन / सेमी है। नली AB का अनुप्रस्थकाट A वर्ग सेमी है। अतः / सेमी चलने में सीमा द्वारा हटाया गया आयतन / A मिलि होगा। यदि HCI के विलयन की सान्द्रता C ग्राम तुल्यांक प्रतिलिटर है तो कैथोड़ की ओर जाने वाले H के ग्राम
हिंदी माध्यम नोट्स
Class 6
Hindi social science science maths English
Class 7
Hindi social science science maths English
Class 8
Hindi social science science maths English
Class 9
Hindi social science science Maths English
Class 10
Hindi Social science science Maths English
Class 11
Hindi sociology physics physical education maths english economics geography History
chemistry business studies biology accountancy political science
Class 12
Hindi physics physical education maths english economics
chemistry business studies biology accountancy Political science History sociology
English medium Notes
Class 6
Hindi social science science maths English
Class 7
Hindi social science science maths English
Class 8
Hindi social science science maths English
Class 9
Hindi social science science Maths English
Class 10
Hindi Social science science Maths English
Class 11
Hindi physics physical education maths entrepreneurship english economics
chemistry business studies biology accountancy
Class 12
Hindi physics physical education maths entrepreneurship english economics