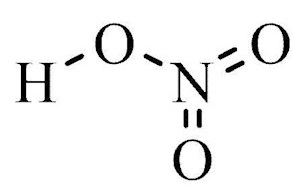नाइट्रिक अम्ल का रासायनिक सूत्र , भौतिक गुण , नाइट्रिक एसिड के उपयोग म अभिक्रिया , गुण (nitric acid in hindi)
(nitric acid in hindi) नाइट्रिक अम्ल का रासायनिक सूत्र , भौतिक गुण , नाइट्रिक एसिड के उपयोग म अभिक्रिया , गुण : यह एक बहुत ही प्रबल अम्ल होता है , नाइट्रिक अम्ल को सूत्र HNO3 द्वारा प्रदर्शित किया जाता है। यह नाइट्रोजन के द्वारा बनाये जाने वाले ओक्सो अम्ल में से एक है , नाइट्रोजन द्वारा निम्न तीन प्रकार के ऑक्सो अम्ल बनाती है –
- नाइट्रस अम्ल (HNO2)
- नाइट्रिक अम्ल (HNO3)
- हाइपोनाइट्रस अम्ल (H2N2O2)
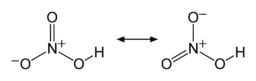
नाइट्रिक अम्ल का सूत्र और संरचना
नाइट्रिक अम्ल बनाने की विधियाँ या विरचन
- NaNO3+H2SO4 → NaHSO4 + HNO3
नाइट्रिक अम्ल के भौतिक गुण
- जब यह शुद्ध अवस्था में होता है तब रंगहीन तेलिय द्रव के समान होता है लेकिन जब इसमें नाइट्रोजन डाइ ऑक्साइड की अशुद्धि मिल जाती है उस स्थिति में इसका रंग पीला भूरा हो जाता है।
- जब इसे पानी में डाला जाता है तो यह पूर्ण रूप से विघटित हो जाता है , इसका जल में हाइड्रोजन आयन और नाइट्रेट आयन के रूप में विघटन हो जाता है।
- जब इस अम्ल को त्वचा पर डाला जाता है तो यह पीड़ादायक घाव बना देता है।
- निर्जलीकृत अम्ल का क्वथनांक 355.6 केल्विन होता है तथा यह लगभग 231.4 केल्विन ताप पर सफ़ेद ठोस के रूप में जम जाता है।
- यह अम्ल विभिन्न सांद्रता वाले विलयन के रूप में मिलता है।
नाइट्रिक अम्ल के रासायनिक गुण
उपयोग
हिंदी माध्यम नोट्स
Class 6
Hindi social science science maths English
Class 7
Hindi social science science maths English
Class 8
Hindi social science science maths English
Class 9
Hindi social science science Maths English
Class 10
Hindi Social science science Maths English
Class 11
Hindi sociology physics physical education maths english economics geography History
chemistry business studies biology accountancy political science
Class 12
Hindi physics physical education maths english economics
chemistry business studies biology accountancy Political science History sociology
English medium Notes
Class 6
Hindi social science science maths English
Class 7
Hindi social science science maths English
Class 8
Hindi social science science maths English
Class 9
Hindi social science science Maths English
Class 10
Hindi Social science science Maths English
Class 11
Hindi physics physical education maths entrepreneurship english economics
chemistry business studies biology accountancy
Class 12
Hindi physics physical education maths entrepreneurship english economics