halogenation of enolizable ketones in hindi इनोल बनाने योग्य कीटोन का हैलोजनीकरण क्या है
इनोल बनाने योग्य कीटोन का हैलोजनीकरण क्या है halogenation of enolizable ketones in hindi ?
इनोल बनाने योग्य कीटोन का हैलोजनीकरण (Halogenation of enolizable ketones)
ऐल्डिहाइड एवं कीटोन में क्रियात्मक समूह के निकटवर्ती C-परमाणु को Q, उससे अगले वाले C- परमाणु को B तथा आगे – y आदि कहते हैं।
पर
इन a –C- परमाणुओं पर उपस्थित हाइड्रोजन परमाणु उपस्थित H–परमाणु B–H कहलाते हैं। इस प्रकार ब्यूटेनैल में दो a-H, दो B – H और तीन में हैं।
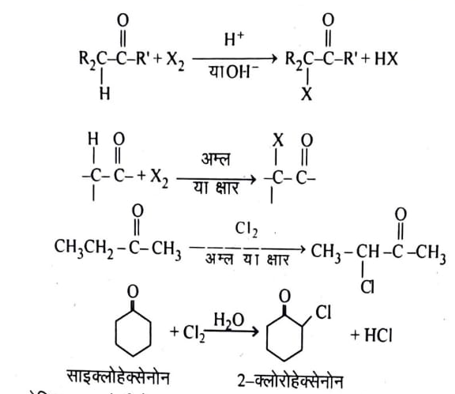
वे ऐल्डिहाइड एवं कीटोन जिनमें a-H परमाणु उपस्थित होते हैं, हैलोजन (X2 = Cl2, Br2 एवं 12) के साथ शीघ्रता से अभिक्रिया करके a- हैलोजन प्रतिस्थापी ऐल्डिहाइड एवं कीटोन बनाते हैं। अर्थात् इनके a-H परमाणु का हैलोजन परमाणु द्वारा प्रतिस्थापन हो जाता है। अभिक्रिया का वेग अम्ल या क्षार की बन जाता है।
ऐल्डिहाइड एवं कीटोन का यह गुण इसके a-H परमाणु की अम्लीय प्रकृति तथा कीटोन की इनॉल बनाने की प्रवृति के कारण है।
(1) क्षार उत्प्रेरित हैलोजनीकरण –
ऐल्डिहाइड एवं कीटोन के क्षार उत्प्रेरित हैलोजनीकरण में इनोलेट आयन या इनोल धीमी गति से बनता है। यह इनोलेट आयन या इनोल हैलोजन के साथ तेजी से अभिक्रिया कर लेता है। ऐल्डिहाइड एवं कीटोन के क्षार उत्प्रेरित हैलोजनीकरण की क्रियाविधि निम्न प्रकार है-
यदि कीटो समूह a-C- परमाणु पर H-परमाणुओं की संख्या अधिक है तो एक से अधिक बार हैलोजनीकरण संभव है। (उदाहरणार्थ- हैलोफार्म अभिक्रिया)
(2) अम्ल उत्प्रेरित हैलोजनीकरण (Acid catalysed halogenation)
ऐल्डिहाइड एवं कीटोन के अम्ल उत्प्रेरित हैलोजनीकरण में पहले गति से इनोल बनता है जो शीघ्रता से हैलोजन से अभिक्रिय कर लेता है।
इस अभिक्रिया की क्रियाविधि निम्न प्रकर है-
a,B- असंतृप्त ऐल्डिहाइड एवं कीटोन (a, B— Unsaturated Aldehydes & Ketones)
ऐसे कार्बोनिल यौगिक (ऐल्डिहाइड अथवा कीटोन) जिनमें कार्बोनिल समूह (>C=O) के a तथा B- कार्बन परमाणुओं के मध्य द्विबन्ध (double bond) उपस्थित होता है, a, B – असंतृप्त कार्बोनिल यौगिक कहलाते हैं। उदाहरणार्थ-
संरचना एवं क्रियाशीलता – a, B- असंतृप्त कार्बोनिल यौगिकों की उपर्युक्त संरचनाओं से स्पष्ट -B है कि कार्बोनिल समूह (>C=O) और ओलिफिनिक समूह ( > C = C<) एक दूसरे के साथ संयुग्मित (Conjugated) है। अतः इनकी अनुनादी संरचनायें होती हैं।
संरचना II एवं III में यद्यपि विपरीत आवेशों का पृथक्करण होता है फिर भी इन संरचनाओं की | महत्वपूर्ण भूमिका है क्योंकि दोनों में ऋणावेश विद्युतऋणी ऑक्सीजन परमाणु पर है।
इन अनुनादी संरचनाओं से स्पष्ट है कि कार्बोनिल समूह की इलेक्ट्रॉन आकर्षी प्रकृति के कारण. | – C = C – बंध के इलेक्ट्रॉन कार्बोनिल समूह द्वारा आकर्षित कर लिये जाते हैं। इस प्रकार इसका लूइस | क्षारक गुण कम हो जाता है और इस पर इलेक्ट्रॉन स्नेही योग कठिनाई से हो पाता है तथा कार्बोनिल | समूह की नाभिक स्नेही अभिक्रियायें सुगमता से हो जाती है।
अनुनादी संरचनाओं से स्पष्ट है कि कार्बन परमाणु- 1 ( कार्बोनिल कार्बन) तथा कार्बन परमाणु-3 (B-C परमाणु ) पर धनावेश है। अतः a, B- असंतृप्त कार्बोनिल यौगिक के अनुनाद संकर को निम्न प्रकार प्रदर्शित कर सकते हैं-
और नाभिक स्नेही योगात्मक अभिक्रियाओं में उत्पादों का मिश्रण प्राप्त होता है। उदाहरणार्थ- HCN योग को एक a. B- असंतृप्त ऐल्डिहाइड पर निम्न प्रकार प्रदर्शित कर सकते हैं-
बनाने की विधियाँ-
a. B- असंतृप्त कार्बोनिल यौगिकों को साधारणतया संगत ऐल्डॉल को गर्म करके बनाया जाता है।
उदाहरणार्थ-
(i) ऐसीटेल्डिहाइड के ऐल्डॉल संघनन से बने उत्पाद को गर्म करने पर क्रोटोनऐल्डिहाइड बनत है ।
(ii) फार्मेल्डिहाइड एवं एसीटोन के मध्य ऐल्डॉल संघनन से बने उत्पाद को गर्म करने पर उसक निर्जलीकरण हो जाता है और मेथिल वाइनिल कीटोन बनता
(iii) ऐसीटोन के ऐल्डोल संघनन से बने उत्पाद को गर्म करने पर मैसिटिल ऑक्साइड (+ मेथिल – 3-पेंटीन-2-ऑन ) बनता है।
a, B असंतृप्त कार्बोनिल यौगिकों की सामान्य अभिक्रियायें – (General chemical reactions of a, B-unsaturated carbonyl compounds)
(1) अपचयन (a) LiAlH, NaBHI, या AlH, से अपचयन करने पर कार्बोनिल समूह द्वितीयक ऐल्कोहॉलिक समूह में बदल जाता है और असंतृप्त ऐल्कोहॉल प्राप्त होते हैं।
(b) Pd–C/H2 से कमरे के ताप पर अपचयन पर संगत संतृप्त एल्डिहाइड एवं कीटोन बनते हैं।
(c) Ni, Pd–C या PrO2 /H2 से उच्च दाब एवं ताप पर अपचयन से संतृप्त ऐल्कोहॉल बनते हैं। द्विबन्ध और कार्बोनिल दोनों समूहों का अपचयन हो जाता है।
(d) Mg-Hg से अम्लीय माध्यम में अपचयन से द्विअणुक उत्पाद बनता है।
(3) हैलोजन अम्लों का योग- a. B- असंतृप्त कीटोन पर हैलोजन अम्लों का योग नाभिक स्नेही आक्रमण द्वारा 1.4-क्रियाविधि प्रयुक्त करके 3. 4- योग होता है।
हाइड्रोजन हैलाइड का योग मार्कोनिकॉफ के नियम के विपरीत होता है उदाहरणार्थ-
(3) हैलोजन का योग – हैलोजन का एक अणु a, B- द्विबन्ध पर जुड़ जाता है।
(4) HCN एवं NaHSO3. का योग HX की भांति ही होता है ।
(5) NH2OH के साथ अभिक्रिया से ऑक्सिम बनते हैं।
यह a, B असंतृप्त कीटोन की महत्वपूर्ण अभिक्रिया है। इसमें a, B – असंतृप्त कीटोन अभिक्रियाशील मेथिलीन समूह वाले यौगिक से क्षार NaOC2H5 की उपस्थिति में अभिक्रिया पर 8- कीटो अम्ल बनाते हैं। यहाँ मेसीटिल ऑक्साइड की मैलोनिक अम्ल के साथ अभिक्रिया का उदाहरण लेते हैं।
इसका जल अपघटन कर गर्म करने पर 8-कीटो अम्ल बनता है परन्तु मेसिटिल ऑक्साइड लेने पर उत्पाद का आन्तरिक क्लेजन संघनन हो जाता है और डाइमीडोन बनता है।
हिंदी माध्यम नोट्स
Class 6
Hindi social science science maths English
Class 7
Hindi social science science maths English
Class 8
Hindi social science science maths English
Class 9
Hindi social science science Maths English
Class 10
Hindi Social science science Maths English
Class 11
Hindi sociology physics physical education maths english economics geography History
chemistry business studies biology accountancy political science
Class 12
Hindi physics physical education maths english economics
chemistry business studies biology accountancy Political science History sociology
English medium Notes
Class 6
Hindi social science science maths English
Class 7
Hindi social science science maths English
Class 8
Hindi social science science maths English
Class 9
Hindi social science science Maths English
Class 10
Hindi Social science science Maths English
Class 11
Hindi physics physical education maths entrepreneurship english economics
chemistry business studies biology accountancy
Class 12
Hindi physics physical education maths entrepreneurship english economics