ferric chloride-water system phase diagram in hindi फैरिक क्लोराइड जल तंत्र क्या है चित्र
फैरिक क्लोराइड जल तंत्र क्या है चित्र सूत्र किसे कहते हैं ferric chloride-water system phase diagram in hindi ?
फैरिक क्लोराइड – जल तंत्र (Ferric Chloride-Water System) अनुसार फैरिक क्लोराइड – जल तंत्र को सर्वप्रथम 1892 में रूजबोम ( Rozebom) ने बताया इसके इसमें चार स्थायी प्रावस्था ठोस डोडेका हाइड्रेट Fe2CI612H2O, हेप्टाहाइड्रेट Fe2 Cl6 7H2O, पेन्टा
हाइड्रेट FeCl6.5H2O व टेट्रा हाइड्रेट Fe2Cl6 4H2O बनते हैं। इसके अलावा एक ठोस प्रावस्था अजलीय (anhydrous) फैरिक क्लोराइड व द्रव प्रावस्था विलयन (Fe2Cl6 + xH2O) पायी जाती है। प्रत्येक प्रावस्था का संघटन दो घटक Fe2Cl6 व H2O है अतः यह द्विघटक तंत्र है। इसमें हाइड्रेट बनता है उसके गलन ताप को सर्वागसम गलन ताप (Congruent melting point) कहते हैं क्योंकि इस बिन्दु पर ठोस हाइड्रेट व द्रव हाइड्रेट में एक सा संघटन होता है।
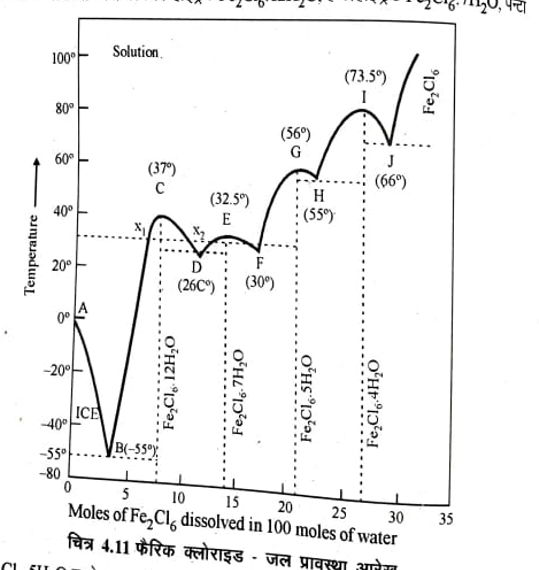
फैरिक क्लोराइड – जल तंत्र के प्रावस्था आरेख को चित्र 4.11 में दर्शाया है।
चारों ठोस हाइड्रेट सर्वांगसम गलन ताप (Congruent melting point ) C ( 37°C). E (32.5°C), G(56°C) तथा 1 (78.5°C) रखते हैं।
बिन्दु A (0°C) पानी का हिमांक बिन्दु है इसमें थोड़ी सी मात्रा Fe2Cl6 की मिलाने पर फैरिक क्लोराइड व जल का विलयन प्राप्त होता है व जल का हिमांक वक्र AB के सहारे कम होता जाता है इस वक्र AB को बर्फ का गलन वक्र कहते हैं तथा यह एक चर है बिन्दु B पर एक नई ठोस प्रावस्था डोडेका हाइड्रेट अलग होती जाती है अतः B (-55°C) पर तीन प्रावस्थाऐं बर्फ, ठोस डोडेका हाइड्रेट तथा विलयन साम्यवस्था में रहते हैं इसको गलन क्रांतिक बिन्दु (Eutectic point) या क्रायोहाइड्रिक बिन्दु (Cryohydric point) कहते हैं । द्विघटक तंत्र के लिए [F=C-P+1=2-3+1= 0 ] यह बिन्दु अचर (nonvariant) है। इस तंत्र में उस बिन्दु पर सबसे कम ताप – 55°C प्राप्त होता है और अधिक ताप बढ़ानेपर विलयन का संघटन वक्र BCD के सहारे परिवर्तित होता है अतः BCD ठोस Fe2Cl6-12H2O का विलेयता वक्र है। व बिन्दु C ठोस Fe2CI612H2O का गलन बिन्दु (melting point) है। वक्र CB व CD वास्तव में क्रमशः जल व फैरिक क्लोराइड के मिलाने पर डोडेका हाइड्रेट के सर्वांगसम गलन ताप में कमी को प्रदर्शित करता है।
बिन्दु D (26°C) पर ठोस हेफ्टाहाइड्रेट (Fe2CI67H2O) अलग होता है व तंत्र अचर होता है। D दूसरा गलन क्रांतिक बिन्दु है इस बिन्दु पर ठोस डोडेका हाइड्रेट, हेफ्टा हाइड्रेट व विलयन तीलप्रावस्थाऐं साम्य में है।
इसी प्रकार F (30°C). H (55°C) वJ (66°C) क्रमश: तीसरा चौथा, व पांचवा गलन क्रान्तिक बिन्दु है
प्रत्येक बिन्दु पर तीन प्रावस्थाऐं क्रमश: हेप्टा हाइड्रेट, पेन्टा हाइड्रेट तथा विलयन (F): पेन्टा हाइड्रेट, टेट्रा हाइड्रेट तथा विलयन (H) और टेट्रा हाइड्रेट, अजलीय Fe2Cl6 तथा विलयन (J) साम्य में रहती है। अजलीय Fe2Cl6 बिन्दु J के ऊपर उपस्थित रहता है। प्रत्येक गलन क्रांतिक बिन्दु पर स्वतंत्रता की कोटि शून्य होती है। Fe2Cl6 जल तंत्र के तापक्रम, संघटन को सारणी 4.6 में प्रदर्शित करते हैं।
हिंदी माध्यम नोट्स
Class 6
Hindi social science science maths English
Class 7
Hindi social science science maths English
Class 8
Hindi social science science maths English
Class 9
Hindi social science science Maths English
Class 10
Hindi Social science science Maths English
Class 11
Hindi sociology physics physical education maths english economics geography History
chemistry business studies biology accountancy political science
Class 12
Hindi physics physical education maths english economics
chemistry business studies biology accountancy Political science History sociology
English medium Notes
Class 6
Hindi social science science maths English
Class 7
Hindi social science science maths English
Class 8
Hindi social science science maths English
Class 9
Hindi social science science Maths English
Class 10
Hindi Social science science Maths English
Class 11
Hindi physics physical education maths entrepreneurship english economics
chemistry business studies biology accountancy
Class 12
Hindi physics physical education maths entrepreneurship english economics
