संघट्ट सिद्धांत (collision theory) , ऊर्जा अवरोधक , अभिविन्यास अवरोधक , अभिक्रिया वेग की ताप पर निर्भरता
- इसके अनुसार किसी अभिक्रिया में अभिकारक अणुओं को ठोस गोले के रूप में माना गया है। इन अभिकारक अणुओं या ठोस गोले के आपस में टक्कराने से अभिक्रिया संपन्न होती है।
- अभिक्रिया मिश्रण के प्रति इकाई आयतन में प्रति सेकंड अभिकारक अणुओं के मध्य होने वाली टक्करो की संख्या संघट्ट आवृति कहलाती है।
- अभिक्रिया में अभिकारक अणुओ के आपस में टक्कराने से अभिक्रिया वेग बढ़ता है लेकिन अभिक्रिया का वेग टक्करो की संख्या बढ़ने के अनुपात में कुछ कम बढ़ पाता है। क्योंकि सभी टक्करे प्रभावी नहीं होती है।
- प्रभावी टक्करो से तात्पर्य अभिकारक अणुओं के उचित अभिविन्यास में टकराने से अर्थात प्रभावी टक्कर से ही अभिकारक अणु उत्पाद में बदल पाते है। अत: किसी रासायनिक अभिक्रिया के संपन्न होने में दो अवरोध पार करने होते है (1) ऊर्जा अवरोधक (2) अभिविन्यास अवरोधक
अत: रासायनिक अभिक्रिया का वेग दो कारको के समानुपाती होता है – पहले संघट्ट आवृत्ति (Z) और दूसरा संघट्ट का अंश (F)
अभिक्रिया वेग = dx/dt = ZF (समीकरण 1)
समीकरण-1 में F = N*/N = e-Ea/RT रखने पर
अभिक्रिया वेग = Ze-Ea/RT (समीकरण-2)
समीकरण 2 , संघट्ट वाद की समीकरण है।
इस समीकरण द्वारा प्राप्त मान सरल अभिक्रियाओ के प्रायोगिक मान से तो मेल खाते है। लेकिन जटिल अभिक्रियाओ के लिए नही।
अत: इस समीकरण को संशोधित करके निम्न समीकरण दी गयी –
अभिक्रिया वेग = P.Ze-Ea/RT (समीकरण-3)
समीकरण 3 संशोधित संघट्टवाद की समीकरण है।
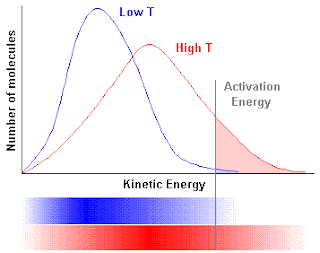
अभिक्रिया वेग की ताप पर निर्भरता
मैक्स वेल वोल्ट्समैन ऊर्जा वितरण वक्र
हिंदी माध्यम नोट्स
Class 6
Hindi social science science maths English
Class 7
Hindi social science science maths English
Class 8
Hindi social science science maths English
Class 9
Hindi social science science Maths English
Class 10
Hindi Social science science Maths English
Class 11
Hindi sociology physics physical education maths english economics geography History
chemistry business studies biology accountancy political science
Class 12
Hindi physics physical education maths english economics
chemistry business studies biology accountancy Political science History sociology
English medium Notes
Class 6
Hindi social science science maths English
Class 7
Hindi social science science maths English
Class 8
Hindi social science science maths English
Class 9
Hindi social science science Maths English
Class 10
Hindi Social science science Maths English
Class 11
Hindi physics physical education maths entrepreneurship english economics
chemistry business studies biology accountancy
Class 12
Hindi physics physical education maths entrepreneurship english economics