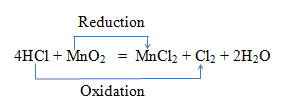ऑक्सीकरण अंक (oxidation number in hindi) , ऑक्सीकरण अंक निकालने के लिए नियम , अनुप्रयोग
ऑक्सीकरण अंक निकालने के लिए स्वेच्छ नियम
, O2 आदि में परमाणु का ऑक्सीकरण अंक शून्य होता है।
2. किसी भी अपरूप में तत्व के प्रत्येक परमाणु का ऑक्सीकरण अंक शून्य होता है।
उदाहरण : हीरे में कार्बन परमाणु , S8 में सल्फर परमाणु का ऑक्सीकरण अंक शून्य होता है।
3. क्षारीय धातुओं का ऑक्सीकरण अंक +1 होता है तथा क्षारीय मृदा धातुओं का ऑक्सीकरण अंक +2 होता है। 4. किसी एक परमाण्विक आयन का ऑक्सीकरण अंक उस पर उपस्थित आवेश की संख्या के बराबर होता है।
जैसे : Cl– , mg2+ , S2- , Al3+ , Na+ आयनों का ऑक्सीकरण अंकक्रमशः -1 , +2 , -2 , +3 , +1 होता है।
5. प्रत्येक यौगिक का ऑक्सीकरण अंक शून्य होता है तथा अणु में बीज गणितीय योग शून्य होता है।
उदाहरण : एक यौगिक का अणुसूत्र AxBy है ,
[X x A तत्व का ऑक्सीकरण अंक ] + [Y x B तत्व का ऑक्सीकरण] = 0
6. बहुपरमाणुक आयन में उपस्थित तत्वों के ऑक्सीकरण अंक का बिजगणितीय योग उस आयन पर उपस्थित आवेश के बराबर होता है।
उदाहरण : एक आयन का अणुसूत्र ABYn- है
[A तत्व का ऑक्सीकरण अंक] + [Y x B तत्व का ऑक्सीकरण अंक] = -n
उदाहरण : [PtCl6]2- में Pt का ऑक्सीकरण अंक ज्ञात कीजिये –
x + (-6) = -2
x – 6 = -2
x = +4
7. सामान्यतया H परमाणु का ऑक्सीकरण अंक +1 होता है।
अपवाद : हाइड्राइडो में H परमाणु का ऑक्सीकरण अंक -1 होता है।
उदाहरण : NaH , LiH , MgH2 , CaH2 आदि में H का ऑक्सीकरण अंक -1 होता है।
8. सामान्यतया यौगिको में O2 का ऑक्सीकरण अंक -2 होता है।
अपवाद 1 : परॉक्साइड में O2 का ऑक्सीकरण अंक -1 होता है।
अपवाद 2 : OF2 में O2 का ऑक्सीकरण अंक +2 होता है।
अपवाद 3 : O2F2 में O2 का ऑक्सीकरण अंक +1 होता है।
9. समस्त यौगिकों में हैलोजन का ऑक्सीकरण अंक -1 होता है।
अपवाद : जिन यौगिको में तत्व (Cu , Br , I) , F व O से जुड़े होते है तो इन तत्वों का ऑक्सीकरण अंक +1 होता है।
10. किसी तत्व का ऑक्सीकरण अंक n से लेकर (n – 8) के मध्य होता है।
जहाँ : n = संयोजकता (बाह्यतम कोश में इलेक्ट्रॉन की संख्या)
उदाहरण : नाइट्रोजन (N) का ऑक्सीकरण अन्क +5 से लेकर -3 के मध्य होता है।
11. ध्रुवीय सहसंयोजक यौगिक में साझे का इलेक्ट्रॉन उस परमाणु के पास माना जाता है जिसकी विद्युत ऋणता अधिक होती है।
उदाहरण : HCl में H का ऑक्सीकरण अंक +1 तथा Cl का ऑक्सीकरण अंक -1 होता है।
12. उपसहसंयोजक यौगिकों में दाता परमाणु का ऑक्सीकरण अंक +2 तथा ग्राही परमाणु का ऑक्सीकरण अंक -2 होता है।
13. किसी अधातु तत्व के धातु अथवा H के साथ बने यौगिक में अधातु तत्व का ऑक्सीकरण ऋणात्मक होता है जबकि धातु तत्व का ऑक्सीकरण अंक धनात्मक होता है।
14. संकर यौगिको में प्रत्येक तत्व के ऑक्सीकरण अंक का मान लगाने की अपेक्षा समूह अथवा मूलको का ऑक्सीकरण अंक लगाना अधिक सुविधाजनक रहता है।
ऑक्सीकरण अंको के आधार पर ऑक्सीकरण -अपचयन
ऑक्सीकरण अंक के अनुप्रयोग
हिंदी माध्यम नोट्स
Class 6
Hindi social science science maths English
Class 7
Hindi social science science maths English
Class 8
Hindi social science science maths English
Class 9
Hindi social science science Maths English
Class 10
Hindi Social science science Maths English
Class 11
Hindi sociology physics physical education maths english economics geography History
chemistry business studies biology accountancy political science
Class 12
Hindi physics physical education maths english economics
chemistry business studies biology accountancy Political science History sociology
English medium Notes
Class 6
Hindi social science science maths English
Class 7
Hindi social science science maths English
Class 8
Hindi social science science maths English
Class 9
Hindi social science science Maths English
Class 10
Hindi Social science science Maths English
Class 11
Hindi physics physical education maths entrepreneurship english economics
chemistry business studies biology accountancy
Class 12
Hindi physics physical education maths entrepreneurship english economics