क्रिस्टलीय ठोसों का वर्गीकरण , क्रिस्टलीय ठोस के प्रकार (classification of crystalline solids in hindi)
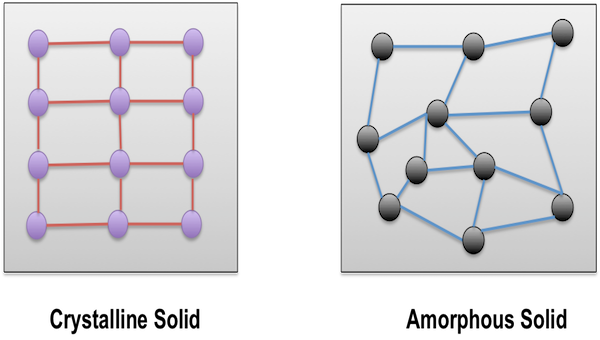
(classification of crystalline solids in hindi) क्रिस्टलीय ठोसों का वर्गीकरण , क्रिस्टलीय ठोस के प्रकार : हम यहाँ क्रिस्टलीय ठोसों के प्रकार के बारे में विस्तार से अध्ययन करेंगे।
4. सहसंयोजक ठोस (Network or Covalent Solids)
1. आण्विक ठोस (Molecular Solids)
i. अध्रुवीय आण्विक ठोस (Non-polar Molecular Solids)
ii. ध्रुवीय आण्विक ठोस (polar Molecular Solids)
iii. हाइड्रोजन आबंधित आणविक ठोस (Hydrogen-Bonded Molecular Solids)
2. आयनिक ठोस (Ionic Solids)
इन आयनों के मध्य अर्थात अवयवी कणों के मध्य विद्युत बल पाए जाते है अर्थात इन अवयवी कण ऋणायन व धनायन के मध्य आकर्षण विद्युत बल पाया जाता है।
उदाहरण : सोडियम क्लोराइड (NaCl) आदि , NaCl में दो प्रकार के आयन पाए जाते है इसमें Na धनायन (Na+) होता है तथा Cl ऋणात्मक (Cl–) आयन रहता है , अत: NaCl को आयनिक ठोस के वर्ग में रखा गया है।
आयनिक ठोसों के निम्न गुण होते है –
ये कठोर और भंगुर प्रकृति के होते है।
इन ठोसों का गलनांक उच्च होता है।
ठोस अवस्था में ये विद्युत के अच्छे चालक नहीं होते है लेकिन पिघलने के बाद या द्रव अवस्था में विद्युत के अच्छे चालक की तरह व्यवहार करते है।
आयनिक ठोस ध्रुवीय विलायक में आसानी से घुल जाते है या विलेयशील होते है।
3. धात्विक ठोस (Metallic Solids)
धात्विक अवयवी कणों के मध्य बहुत अधिक मजबूत धात्विक बंध पाए जाते है।
चूँकि इन ठोसों में मुक्त इलेक्ट्रॉन पाए जाते है और मुक्त गति करते रहते है इसलिए धात्विक ठोस विद्युत के सुचालक होते है अर्थात धात्विक ठोसों में विद्युत का चालन आसानी से हो पाता है।
उदाहरण : जिंक , सोना आदि धात्विक ठोस के उदाहरण है।
धात्विक ठोसों में निम्न गुण पाए जाते है –
धात्विक ठोसों का गलनांक और क्वथनांक उच्च होता है।
ये विद्युत के और ऊष्मा के बहुत अच्छे चालक होते है , क्यूंकि इनमें मुक्त इलेक्ट्रॉन बहुत अधिक पाए जाते है।
ये ठोस अत्यधिक आघातवर्धनीय और तन्य प्रकृति के होते है और इनकी इसी प्रकृति या गुण के कारण इनका उपयोग चदरें बनाने और तार खींचे जाने के लिए किया जाता है।
4. सहसंयोजक ठोस (Network or Covalent Solids)
हिंदी माध्यम नोट्स
Class 6
Hindi social science science maths English
Class 7
Hindi social science science maths English
Class 8
Hindi social science science maths English
Class 9
Hindi social science science Maths English
Class 10
Hindi Social science science Maths English
Class 11
Hindi sociology physics physical education maths english economics geography History
chemistry business studies biology accountancy political science
Class 12
Hindi physics physical education maths english economics
chemistry business studies biology accountancy Political science History sociology
English medium Notes
Class 6
Hindi social science science maths English
Class 7
Hindi social science science maths English
Class 8
Hindi social science science maths English
Class 9
Hindi social science science Maths English
Class 10
Hindi Social science science Maths English
Class 11
Hindi physics physical education maths entrepreneurship english economics
chemistry business studies biology accountancy
Class 12
Hindi physics physical education maths entrepreneurship english economics

