उपसहसंयोजक यौगिको में आबन्धन , VBT – valence bond theory (संयोजकता बंध सिद्धांत) , VBT – valence bond theory (संयोजकता बंध सिद्धांत)
उपसहसंयोजक यौगिको में आबन्धन : उपसहसंयोजक यौगिको में केन्द्रीय धातु आयन व लिगेंड के मध्य आबंधन को समझाने के लिए निम्न सिद्धांत दिए गए।
1. VBT – valence bond theory (संयोजकता बंध सिद्धांत)
2. CFT – crystal field theory (क्रिस्टल क्षेत्र सिद्धांत)
3. LFT – legend field theory
4. MOT – molecular orbital theory
1. VBT – valence bond theory (संयोजकता बंध सिद्धांत)
2. CFT – crystal field theory (क्रिस्टल क्षेत्र सिद्धांत)
3. LFT – legend field theory
4. MOT – molecular orbital theory
1. VBT – valence bond theory (संयोजकता बंध सिद्धांत)
यह सिद्धान्त पॉलिंग ने दिया था , इस सिद्धांत के आधार पर संकुल यौगिको की आकृति व इसके चुम्बकीय गुणों की व्याख्या की जाती है।
इस सिद्धांत के मुख्य बिंदु निम्न है –
इस सिद्धांत के मुख्य बिंदु निम्न है –
- सर्वप्रथम केन्द्रीय धातु परमाणु अपनी ऑक्सीकरण अवस्था के अनुरूप इलेक्ट्रॉन त्याग कर धनायन बनाता है।
- इस धातु धनायन के पास लिगेंड को जोड़ने के लिए रिक्त s,p,d कक्षक उपलब्ध होते है।
- यह रिक्त कक्षक आपस में मिलकर संकरित कक्षकों का निर्माण करते है।
- इन रिक्त संकरित कक्षको में लिगेंड अपना एकांकी इलेक्ट्रोन युग्म प्रदान करके धातु आयन के साथ बंध बना लेता है।
- इसी संकरण के आधार पर संकुल यौगिक की ज्यामिति निर्धारित होती है –
|
संकरण
|
ज्यामिति
|
|
SP3
|
चतुष्फलकीय
|
|
dsp2
|
वर्ग समतलीय
|
|
d2sp3
|
अष्टफलकीय (बाह्य
कक्षक संकुल) |
|
Sp3d2
|
अष्टफलकीय (आन्तरिक
कक्षक संकुल) |
- यदि संकरण में आन्तरिक d कक्षक भाग लेते है तो आंतरिक कक्षक संकुल बनता है लेकिन यदि संकरण में बाह्य d कक्षक भाग ले तो बाह्य कक्षक संकुल बनता है। आंतरिक कक्षक संकुल / चक्रण युग्मित संकुल / निम्न चक्रण संकुल।
- बाह्य कक्षक संकुल / चक्रण मुक्त संकुल / उच्च चक्रण संकुल।
- यदि धातु आयन के असंकरित कक्षकों में सभी इलेक्ट्रोन युग्मित हो तो वह यौगिक प्रतिचुम्बकीय होगा , लेकिन यदि अयुग्मित इलेक्ट्रोन उपस्थित हो तो वह यौगिक अनुचुम्बकीय होगा।
- यौगिक के चुम्बकीय आघूर्ण के मान को निम्न सूत्र द्वारा ज्ञात कर सकते है –
यहाँ n = अयुग्मित इलेक्ट्रोन की संख्या
- यदि अयुग्मित इलेक्ट्रोन उपस्थित हो तो वह यौगिक रंगीन होगा तथा यदि अयुग्मित इलेक्ट्रोन अनुपस्थित हो तो वह यौगिक रंगहीन होगा।
प्रबल लिगेंड : NH3 , en , CN , CO
दुर्बल लिगेंड होने पर इलेक्ट्रोन का युग्मन नहीं होगा।
प्रबल लिगेंड होने पर इलेक्ट्रॉन के युग्मन की संभावना होगी।
उदाहरण : [CO(NH3)6]3+
CO का इलेक्ट्रॉनिक विन्यास :- [Ar] 3d7 4s2 4p0
CO की ऑक्सीकरण संख्या : +3
CO3+ का इलेक्ट्रॉनिक विन्यास : [Ar] 3d6 4s0 4p0
संकरण :- d2sp3
आकृति : अष्टफलकीय
संकुल : आंतरिक कक्षक संकुल
चुम्बकीयता : प्रति चुम्बकीय
चुम्बकीय आघूर्ण : n = 0 तो 0 BM
रंग : रंगहीन
2. CFT – crystal field theory (क्रिस्टल क्षेत्र सिद्धान्त)
यह सिद्धांत बैथे नामक वैज्ञानिक ने दिया। इस सिद्धान्त के मुख्य बिंदु निम्न है –
- यह सिद्धांत सर्वप्रथम आयनिक क्रिस्टलो पर लागू किया गया इसलिए इसे क्रिस्टल क्षेत्र सिद्धांत कहते है।
- इस सिद्धांत के अनुसार केंद्रीय धातु आयन व लिगेंड आपस में स्थिर विद्युत आकर्षण बल या आयनिक बंध द्वारा बंधित होते है।
- यह स्थिर विद्युत आकर्षण बल , केन्द्रीय धातु आयन के धनावेश व लिगेंड के ऋण आवेश के कारण उत्पन्न होता है।
- यदि लिगेंड उदासीन हो तो वह द्विध्रुव की तरह व्यवहार करता है तथा उस लिगेंड का ऋण आवेशित सिरा धातु आयन की ओर विन्यासित होता है।
- केन्द्रीय धातु आयन के पास उपस्थित पाँचो d कक्षको की ऊर्जा एक समान होती है इसलिए इन्हें समभ्रंश d कक्षक कहते है।
- इस सिद्धान्त के अनुसार जब लिगेंड धातु आयन से जुड़ने के लिए धातु आयन की ओर अग्रसर होते है तो यह धातु आयन के d कक्षकों की ऊर्जा को प्रभावित करते है जिससे धातु आयन के यह d कक्षक दो भागो में बंट जाते है – (i) t2g कक्षक (ii) eg कक्षक
- यह घटना क्रिस्टल फिल्ड विपाटन कहलाती है तथा इन t2g व eg कक्षकों के मध्य ऊर्जा के अन्तर को क्रिस्टल फिल्ड विपाटन ऊर्जा कहते है।
d कक्षकों के प्रकार : मुख्य रूप से यह दो प्रकार के होते है –
(i) t2g कक्षक : इनकी पालियां अक्षो के मध्य स्थित होती है। ये तीन प्रकार के होते है।
(a) dxy (b) dyz (c) dxz
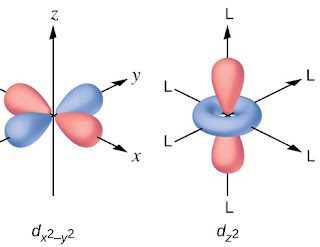
(ii) eg कक्षक : इनकी पालियाँ अक्षो के ऊपर होती है। ये दो प्रकार के होते है –
(a) dx2y2 (b) dz2
अष्टफलकीय संकुलों में क्रिस्टल फिल्ड विपाटन
अष्टफलकीय संकुलों में लिगेंड धातु आयन से जुड़ने के लिए अक्षो के ऊपर से अग्रसर होते है अत: धातु आयन के eg कक्षक (जिनकी पालियाँ अक्षों के ऊपर होती है ) लिगेंड के मार्ग में आ जाते है इस कारण eg कक्षक की पालियो में उपस्थित इलेक्ट्रोन व लिगेंड के इलेक्ट्रोन के मध्य प्रतिकर्षण होता है जिसके फलस्वरूप विपाटन होने से eg कक्षकों की ऊर्जा अधिक एवं t2g कक्षकों की ऊर्जा कम हो जाती है इस प्रकार अष्टफलकीय संकुलों में क्रिस्टल फिल्ड विपाटन होता है।
अष्टफलकीय संकुलों में क्रिस्टल फिल्ड विपाटन ऊर्जा को △0 से दर्शाते है। इसमें विपाटन के दौरान eg कक्षकों की ऊर्जा 0.6 △0 बढ़ जाती है एवं t2g कक्षकों की ऊर्जा 0.4△0 कम हो जाती है।
स्पेक्ट्रो रासायनिक श्रेणी
भिन्न भिन्न लिगेंडो को उनकी प्रबलता के बढ़ते क्रम में व्यवस्थित करने पर जो श्रेणी प्राप्त होती है , उसे स्पेक्ट्रो रासायनिक श्रेणी कहते है।
ये श्रेणी निम्न प्रकार से है –
I– < Br– < SCN < Cl– < N3- < NO3–< F– < OH– < C2O42-< H2O < NCS– < edta4- < H–< NH3 < en < CN– < NO2–< CO3
अष्टफलकीय संकुलों में भिन्न भिन्न विन्यास वाले धातु आयन के d कक्षको इलेक्ट्रॉन का वितरण : अष्टफलकीय संकुलों में धातु आयन के d कक्षकों में इलेक्ट्रोन का वितरण क्रिस्टल फिल्ड विपाटन ऊर्जा (△0) व युग्मन ऊर्जा (p) पर निर्भर करता है। इसमें दो स्थितियाँ बनती है –
स्थिति प्रथम [△0 < P]
दुर्बल क्षेत्र लिगेंड होगा।
इलेक्ट्रॉन का युग्मन नहीं होगा।
बाह्य कक्षक संकुल / उच्च चक्रण संकुल बनेगा।
उदाहरण : d6 विन्यास (दुर्बल क्षेत्र लिगेंड)
स्थिति द्वितीय [△0 > P]
प्रबल क्षेत्र लिगेंड होगा।
इलेक्ट्रोन का युग्म होगा।
आन्तरिक कक्षक संकुल / निम्न चक्रण संकुल बनेगा।
उदाहरण : d6 विन्यास (प्रबल क्षेत्र लिगेंड )
चतुष्फलकीय संकुलों में क्रिस्टल फिल्ड विपाटन
चतुष्फलकीय संकुलों में लिगेंड धातु आयन से जुड़ने के लिए अक्षों के मध्य से अग्रसर होते है।
अत: धातु आयन के t2g कक्षक (जिनकी पालियां अक्षों के मध्य होती है ) लिगेंड के मार्ग में आ जाते है इस कारण t2g कक्षक की पालियो में उपस्थित इलेक्ट्रोन व लिगेंड के इलेक्ट्रॉन के मध्य प्रतिकर्षण होता है जिसके फलस्वरूप विपाटन से t2g कक्षकों की ऊर्जा अधिक एवं eg कक्षकों की ऊर्जा कम हो जाती है। इस प्रकार चतुष्फलकीय संकुलों में क्रिस्टल फिल्ड विपाटन होता।
इन संकुलों में क्रिस्टल पिण्ड विपाटन ऊर्जा को △t से दर्शाते है। विपाटन के दौरान t2g कक्षकों की ऊर्जा 0.4△t बढ़ जाती है एवं eg कक्षकों की ऊर्जा 0.6△t कम हो जाती है।
चतुष्फलकीय संकुलों में क्रिस्टल फिल्ड ऊर्जा का मान कम होता है अत: इसमें निम्न स्थिति बनती है –
स्थिति प्रथम :
[△t < P]
दुर्बल क्षेत्र लिगेंड होगा।
इलेक्ट्रॉन का युग्मन नहीं होगा।
उच्च चक्रण संकुल