pinacol pinacolone rearrangement in hindi पिनेकॉल पिनेकोलॉन पुनर्विन्यास पिनाकोल पिनाकोलोन पुनर्व्यवस्था की व्याख्या करें
पिनाकोल पिनाकोलोन पुनर्व्यवस्था की व्याख्या करें pinacol pinacolone rearrangement in hindi पिनेकॉल पिनेकोलॉन पुनर्विन्यास क्या है ?
पिनेकॉल-पिनेकोलॉन पुनर्विन्यास (Pinacol-Pinacolone Rearrangement)
कटवर्ती तृतीयक C- परमाणु पर दो ऐल्कोहॉलिक – OH समूह उपस्थित होने पर बने 1,2- डाइऑल पिनेकॉल कहलाते हैं। सरतलम पिनेकॉल 2,3 – डाइमेथिल ब्यूटेन -2, 3 – डाइऑल Me, C(OH). (C(OH) Me♭ है। यह तुन H2SO4 की उपस्थिति में पिनेकोलॉन MeC – C -Me में पुनविन्यसित हो जाता है। इस पुनर्विन्यास को पिनेकॉल पिनेकोलॉन पुनर्विन्यास कहते हैं। यह एक 1,2-विस्थापन है।
क्रियाविधि – अभिक्रिया की क्रियाविधि निम्नलिखित पदों में दी जा सकती है-
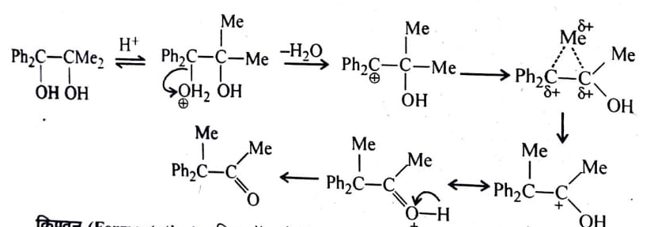
पद (1): हाइड्रॉक्सी समूह का उत्क्रमणीय प्रोटॉनीकरण और जल के अणु का विलोपन इसमें इलेक्ट्रॉन न्यून कार्बोधनायन बनता है।
पद (2) मध्यवर्ती सेतुंकार्बनिक आयन का बनना- – उपर्युक्त कार्बोधनायन मध्यवर्ती सेतु कार्बोनियम आयन में बदल जाता है। इसलिये यह एक अन्तः अणुक पुनर्विन्यास है अभिगामी (-CH3) समूह सबस्ट्रेट से पृथक नहीं होता है ।
पद (3) : पूर्ण अभिगमन के पश्चात् प्राप्त कार्बोधनायन का अनुनाद द्वारा स्थिरीकरण हो जाता है।
पद 4- उपर्युक्त कार्बोधनायन से प्रोटॉन निकल कर ऑक्सो यौगिक पिनेकोलॉन बन जाता है-
विभिन्न प्रकार के पिनेकॉल में अभिगामी समूहों के विस्थापन का क्रम निम्न प्रकार है-
Ph> (CH3)3C>CH3CH 2-CH 3
परन्तु में अभिगामी समूह Ph न होकर Me है और निम्न प्रकार अभिक्रिया प्रारंभ होती
किण्वन (Fermentation) :- ग्लिसरॉल के किण्वण से कई प्रकार के यौगिक जैसे प्रोपेनोइक अम्ल, n-ब्यूटेनोइक अम्ल, लेक्टिक अम्ल, ट्राइमेथिलीन ग्लाइकॉल, सक्सीनिक अम्ल, n – ब्यूटेनोल आदि का निर्माण होता है। विशिष्ट प्रकार के यौगिक के निर्माण में विशिष्ट प्रकार के बैक्टीरिया की भूमिका होती है। उदाहरणार्थ, बेसिलस ब्यूटिलिकस बैक्टीरिया से n – ब्यूटिरिक अम्ल का निर्माण होता है। उपयोग : एथिलीन ग्लाइकोल के उपयोग निम्नलिखित हैं-
(i) विलायक के रूप में
(ii) टेरिलीन, विस्कॉस रेयान, पॉलीयूरेथेन बहुलक, डाइऑक्सेन, डाइऐथिलीन ग्लाइकॉल आदि के निर्माण में
(iii) एथिलीन ग्लाइकॉल डाइनाइट्रेट, ट्राइनाइट्रोग्लिसरीन के साथ फास्फेट के रूप में प्रयुक्त होता है।
(iv) वायुयानों के पंखों पर बर्फ के बनने या जमने से रोकने लिये हिम विरोधी के रूप में
(v) विद्युत संघनित्रों में डाइइलेक्ट्रिक के रूप में।
ट्राइहाइड्रिक ऐल्कोहॉल (Trihydric Alcohol)
नामकरण – जैसा कि ऊपर बताया जा चुका है ट्राइहाइड्रिक ऐल्कोहॉल में तीन OH समूह भिन्न-भिन्न C-परमाणुओं पर उपस्थित होते हैं और नामकरण की IUPAC प्रणाली में इन्हें ऐल्केन ट्राइऑल कहते हैं। ट्राईऑल से पूर्व श्रृंखला पर – OH समूहों की स्थिति को दर्शाते हैं। यदि श्रृंखला में अन्य ऐल्किल प्रतिस्थापी उपस्थित हैं तो उन्हें नाम से पूर्व अंग्रेजी वर्णमाला के क्रम में श्रृंखला पर उनकी स्थिति दर्शाते हुये लिख देते हैं । उदाहरणार्थ-
ट्राइहाइड्रिक ऐल्कोहॉल मे केवल ग्लिसरॉल (प्रोपेन – 1, 2, 3 – ट्राइऑल) ही महत्वपूर्ण है। अतः हम यहाँ ग्लिसरॉल का ही वर्णन करेंगे। ग्लिसरॉल सभी वसा एवं तेलों में उच्च वसा अम्लों जैसे पामिटिक अम्ल स्टिरिक अम्ल एवं ओलेइक अम्लों के ग्लिसारेल एस्टर के रूप में उपस्थित होता है।
ट्राइहाइड्रिक ऐल्कोहॉल ( ग्लिसरॉल) के बनाने की विधियाँ-
1. तेल एवं वसा के साबुनीकरण से (Saponification of oils and fats )
वसा तथा तेल उच्च वसा अम्लों के ग्लिसरॉल के साथ बने ट्राइएस्टर होते हैं। इनका कॉस्टिक सोडा (NaOH) से जलअपघटन करने पर ग्लिसरॉल बनता है।
इस अभिक्रिया का उपयोग साबुन बनाने में करते हैं। ग्लिसरॉल तो उपजात (by Product) के रूप में प्राप्त होता है।
2. प्रोपिलीन से – औद्योगिक रूप इसका संश्लेषण प्रोपिलीन से करते हैं।
3. प्रोपिलीन से ग्लिसरॉल को निम्न अभिक्रिया अनुक्रम के द्वारा प्राप्त किया जा सकता है-
ग्लिसरॉल की रासायनिक अभिक्रियाऐं (Chemical reactions of glycerol)
ग्लिसरॉल मे दो प्राथमिक एवं एक द्वितीयक ऐल्कोहॉलिक समूह उपस्थित है। यह इन दोनों प्रकार के ऐल्कोहॉलों की रासायनिक अभिक्रियाऐं देता है। ग्लिसरॉल के C-परमाणुओं को निम्न प्रकार प्रदर्शित करते हैं।
ग्लिसरॉल की कुछ मुख्य रासायनिक अभिक्रियाऐं निम्न प्रकार हैं-
(1) सोडियम धातु के साथ – 298 K पर सोडियम ग्लिसरॉल के प्रथम प्राथमिक ऐल्कोहॉलिक समूह से और 373K पर दूसरे प्राथमिक ऐल्कोहॉलिक समूह से अभिक्रिया करके H2 गैस मुक्त करता है।
द्वितीयक ऐल्कोहॉलिक समूह की Na से कोई अभिक्रिया नहीं हो पाती । (2) हैलोजन अम्लों के साथ-
(i) हाइड्रोजन क्लोराइड के साथ – 383K पर ग्लिसरॉल एवं HCI गैस (1 : 1) अभिक्रिया करके a- एवं B- ग्लिसरॉलमोनोक्लोरोहाइड्रिन का मिश्रण बनाते हैं । इसी ताप पर 25% अतिरिक्त HCI गैस से अभिक्रिया पर a,B’-डाइक्लोरोहाइड्रिन (a – डाइक्लोरोहाइड्रिन) तथा a, B- डाइक्लोरोहाइड्रिन (B डाइक्लोरोहाइड्रिन) का मिश्रण प्राप्त होता है ।
(ii) HBr के साथ – HBr के साथ ग्लिसरॉल की अभिक्रिया HCI के समान ही होती है।
(iii) HI के साथ— (a) HI की थोड़ी मात्रा या PI3 के साथ अभिक्रिया पर ऐलिल आयोडाइड बनता
(b) HI की अधिकता के साथ-
उपर्युक्त पद में प्राप्त ऐलिल आयोडाइड आगे फिर HI से अभिक्रिया करके आइसोप्रोपिल आयोडाइड बनाता
है।
(3) सांद्र नाइट्रिक अम्ल के साथ- सांद्र H2SO4 की उपस्थिति में सांद्र नाइट्रिक अम्ल के साथ अभिक्रिया पर ग्लिसरोलट्राइनाइट्रेट या नाइट्रोग्लिसरीन बनता है ।
ग्लिसरिल नाइट्रेट एक रंगहीन तैलीय द्रव है। इसे अल्फ्रेड नोबेल के नाम से नोबेल तेल (Noble oil) भी कहते हैं। यह कीजेलगुहर जो कि विशेष प्रकार की मृदा है पर अवशोषित होकर विस्फोटक पदार्थ डाइनेमाइट (dynamite) बनाता है।
आजकल लकड़ी की लुगदी पर ग्लिसरिलट्राइनाइट्रेट को अवशोषित करते हैं और उसमें ठोस अमोनियम नाइट्रेट मिलाकर डायनेमाइट बनाते है। विस्फोटक जिलेटिन या जेलिगनाइट को बनाने के लिये ग्लिसरिलट्राइनाइट्रेट को गन कॉटन (सैलुलोस नाइट्रेट) के साथ मिश्रित करते हैं। ग्लिसरिल ट्राइनाइट्रेट, गनकॉटन तथा वेस्लीन का मिश्रण धुयें रहित चूर्ण कोरडाइट ( Chordite) होता है ।
(4) फॉस्फोरस हैलाइड के साथ- (i) PCI3 एवं PCI5 दोनों ही ग्लिसरॉल के साथ अभिक्रिया करके 1,2,3 – ट्राइक्लोरोप्रोपेन बनाते हैं।
(ii) PBr3 की अभिक्रिया भी PCI3 की तरह ही होती है और 1, 2, 3- ट्राइब्रोमोप्रोपेन बनता है।
(iii) PI3 की अभिक्रिया थोड़ी सी मात्रा में HI के साथ अभिक्रिया के समान होती है और ऐलिल आयोडाइड बनता
(5) निर्जलीकरण – KHSO4 के साथ अभिक्रिया – ग्लिसरॉल को निर्जल KHSO4 या ZnCI2 या
सांद्र H2SO4 या P2O5 के साथ गर्म करने पर इसका निर्जलीकरण हो जाता है।
(6) कार्बनिक मोनोकार्बोक्सिलिक अम्लों के साथ अभिक्रिया करके मोनो, डाइ एव ट्राइ एस्टर बनते हैं। यह अभिक्रिया के ताप एवं अम्ल की प्रयुक्त मात्रा पर निर्भर करता है।
(7) ऐसीटिलीकरण- ग्लिसरॉल की अभिक्रिया ऐसीटिकऐनहाइड्राइड या ऐसीटिल क्लोराइड के साथ करने पर ग्लिसरॉलट्राइऐसीटेट बनता है।
(8) ऑक्सलिक अम्ल के साथ-
(i) 383K ताप पर – यह ऑक्सेलिक अम्ल के साथ 383K ताप पर अभिक्रिया करके पहले ग्लिसरॉल मोनोऑक्सेलेट बनाता है जो CO2 अणु को त्यागकर ग्लिसरॉलमोनोफॉर्मेट में बदल जाता है जो जल अपघटन पर फॉर्मिक अम्ल और पुनः ग्लिसरॉल बनाता है। इस अभिक्रिया का उपयोग फॉर्मिक अम्ल बनाने में करते हैं।
(ii) 503 K ताप पर – यह ऑक्सेलिक अम्ल के साथ 503K ताप पर अभिक्रिया करके पहले ग्लिसरॉलडाइऑक्सेलेट बनाता है जो कार्बनडाइऑक्साइड के दो अणु त्याग कर ऐलिल ऐल्कोहॉल देता है
9. ऑक्सीकरण – ग्लिसरॉल के ऑक्सीकरण विभिन्न ऑक्सीकारकों से करने पर विभिन्न उत्पाद प्राप्त होते हैं। ग्लिसरॉल के ऑक्सीकरण के अनुक्रम को निम्न प्रकार प्रदर्शित कर सकते हैं-
(i) तनु HNO3 से ऑक्सीकरण पर मुख्यतः (B) एवं (C) बनते हैं।
(ii) सान्द्र HNO3 से ऑक्सीकरण पर मुख्यतः (B) बनता है। (iii) बिस्मथनाइट्रेट से ऑक्सीकरण पर मुख्यतः (E) बनता है।
(iv) ब्रोमीन जल या सोडियम हाइपोब्रोमाइट या फेन्टन अभिकर्मक (Fe2+ + H2O2) से ऑक्सीकरण पर A तथा D का मिश्रण प्राप्त होता है जिसे ग्लिसरोस कहते हैं।
A तथा D निर्जल पिरिडीन की उपस्थिति में अन्तर्परिवर्तित हो जाते हैं। इसे लोरोब्राउन आइकस्टीन पुनर्विन्यास कहते हैं।
10. ऑक्सीकरणी विदलन (Oxidative Cleavage)- (i) परआयोडिक अम्ल से ऑक्सीकरण पर फॉर्मेल्डिहाइड एवं फॉर्मिक अम्ल बनते हैं।
(ii) अम्लीय KMnO4 से ऑक्सीकरण पर ऑक्सेलिक अम्ल बनता है।
11. बेंजेल्डिहाइड से- बेंजेल्डिहाइड से अभिक्रिया पर चक्रीय ईथर बनता है।
12. ट्राईफेनिल मेथिलक्लोराइड के साथ – ट्राइफेनिलमेथिलक्लोराइड या ट्राइटिलक्लोराइड (C6H5)3C–CI के साथ अभिक्रिया पर प्राथमिक ऐल्कोहॉल समूहों का ही ईथरीकरण होता है।
13.ग्लिसरॉल का विभिन्न यौगिकों में किण्वन हो जाता है। उदाहरणार्थ- प्रोपेनोइक अम्ल बैक्टीरिया से प्रोपिऑनिक अम्ल, सक्सिनिक अम्ल तथा ऐसीटिक अम्ल बनते हैं ।
उपयोग (Uses) :-
ग्लिसरॉल के उपयोग निम्नलिखित हैं-
(i) ग्लिसरॉल ट्राइनाइट्रेट (नाइट्रोग्लिसरीन) बनाने में, इसे नोबेल आयल भी कहते हैं। यह आघात के प्रति संवेदनशील होता है। अतः इसमें कई विस्फोटक पदार्थ बनाये जाते हैं। नाइट्रोग्लिसरीन को लकड़ी के बुरादे में सोखकर तथा अमोनियम नाइट्रेट मिलाकर डायनामाइट बनाया जाता है। नाइट्रोग्सिरीन तथ गनकॉटन (सेलुलोस नाइट्रेट) के मिश्रण से विस्फोटक जिलैटिन प्राप्त होता है। नाइट्रोग्लिसरीन सेलुलोस नाइट्रेट तथा वैसलीन के मिश्रण को कार्डाइट कहते हैं।
(ii) मृदुकारक एवं आर्द्रताग्राही के रूप में ।
(iii) अम्लरोधी सीमेन्ट बनने में ।
(iv) स्नेहक के रूप में ।
(v) बूट पॉलिश, सौन्दर्य प्रसाधन में विलायक के रूप में।
(vi) हिमरोधी के रूप में
हिंदी माध्यम नोट्स
Class 6
Hindi social science science maths English
Class 7
Hindi social science science maths English
Class 8
Hindi social science science maths English
Class 9
Hindi social science science Maths English
Class 10
Hindi Social science science Maths English
Class 11
Hindi sociology physics physical education maths english economics geography History
chemistry business studies biology accountancy political science
Class 12
Hindi physics physical education maths english economics
chemistry business studies biology accountancy Political science History sociology
English medium Notes
Class 6
Hindi social science science maths English
Class 7
Hindi social science science maths English
Class 8
Hindi social science science maths English
Class 9
Hindi social science science Maths English
Class 10
Hindi Social science science Maths English
Class 11
Hindi physics physical education maths entrepreneurship english economics
chemistry business studies biology accountancy
Class 12
Hindi physics physical education maths entrepreneurship english economics