difference between primary secondary and tertiary alcohols प्राथमिक द्वितीयक तृतीयक अल्कोहल में विभेद कीजिए
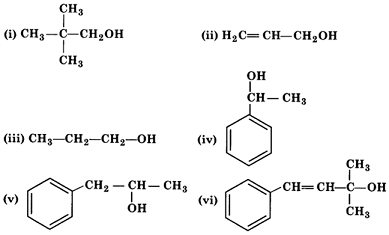
प्राथमिक द्वितीयक तृतीयक अल्कोहल में विभेद कीजिए difference between primary secondary and tertiary alcohols in hindi ?
ऐल्कोहॉल का ऑक्सीकरण (Oxidation of alcohols)
(1) प्राथमिक (1°) ऐल्कोहॉल का ऑक्सीकरण– प्राथमिक ऐल्कोहॉल ऑक्सीकरण पर पहले समान कार्बन युक्त ऐल्डिहाइड देते हैं जो आगे ऑक्सीकृत होकर समान कार्बन युक्त अम्लों में बदल जाते हैं। ऐल्डिहाइड या अम्ल का बनना ऑक्सीकारक की प्रकृति पर निर्भर करता है ।
साधारणतया प्राथमिक ऐल्कोहॉल से ऐल्डिहाइड बनाने के लिए इसका ऑक्सीकरण निम्न प्रकार करते हैं।
(i) N-ब्रोमोसक्सिनीमाइड से – N – ब्रोमोसक्सिनीमाइड प्राथमिक ऐल्केनॉल को ऐल्केनैल में ऑक्सीकृत कर देता है।
(ii) सेरेट कोलिन्स अभिकर्मक (Seret Collin’s reagent) द्वारा प्राथमिक ऐल्केनॉल का ऑक्सीकरण क्रोमियम ट्राइऑक्साइड और पिरिडीन मिश्रण (सेरेट कोलिन्स अभिकर्मक) द्वारा करने पर केवल ऐल्केनल बनते हैं।
(iii) प्राथमिक ऐल्केनॉल का ऐल्केनैल में ऑक्सीकरण करने के लिए पिरिडीनियम क्लोरोक्रोमेट (C6H5NH+ CrO3CI) ऑक्सीकारक का उपयोग करते हैं। इसे क्रोमिक अम्ल तथा पिरिडीनियम क्लोराइड की अभिक्रिया द्वारा बनाया जा सकता है।
(iv) प्राथमिक ऐल्केनॉल का ऐल्केनैल में ऑक्सीकरण, ऐल्केनॉल वाष्प और वायु के मिश्रण को 250°C ताप पर तप्त रजत पर से प्रवाहित करने पर भी किया जा सकता है।
(v) ओपेनॉअर (Oppenauer, 1949) के अनुसार तृतीयक ब्यूटिल क्रोमेट (तृतीयक ब्यूटेनॉल में क्रोमियम ट्राइऑक्साइड मिलाने से बनता है) प्राथमिक ऐल्केनॉल को ऐल्केनैल की मात्रात्मक लब्धि में ऑक्सीकृत कर देता है।
(vi) प्राथमिक ऐल्कोहॉल का विहाइड्रोजनीकरण (ऑक्सीकरण Cu के साथ 300°C पर गर्म करके भी किया जा सकता है।
सोडियम या पोटैशियम डाइक्रोमेंट और सांद्र H2SO4 के मिश्रण से ऑक्सीकरण करने पर पहले समान कार्बन परमाणु युक्त ऐल्डिहाइड और फिर समान कार्बन परमाणु युक्त कार्बोक्सिलिक अम्ल प्राप्त होते हैं।
(2) द्वितीयक (2°) ऐल्कोहॉल का ऑक्सीकरण – द्वितीयक ऐल्कोहॉल का ऑक्सीकरण होने पर कीटोन बनते हैं। साधारणतया अभिक्रिया इसी स्थिति पर रुक जाती है क्योंकि कीटोन का ऑक्सीकरण कठिन होता है। द्वितीयक ऐल्कोहॉल को कीटोन में ऑक्सीकृत करने के लिए N- ब्रोमोसक्सिनिमाइड, सोडियम डाइ क्रोमेट-सांद्र H2SO4 आदि ऑक्सीकारक काम में लेते हैं।
ओपेनॉअर ऑक्सीकरण (Oppenauer oxidation)– द्वितीयक ऐल्कोहॉल को एक विशिष्ट अभिकर्मक ऐलुमिनियम तृतीयक ब्यूटॉक्साइड [(CH3)3 – C– O]3AI की उपस्थिति में प्रोपेनोन की अधिकता के साथ पश्चवाहन करने पर उसका ऐल्केनोन में ऑक्सीकरण हो जाता है। यह अभिक्रिया ओपेनॉअर ऑक्सीकरण कहलाती है।
जलीय ऐसीटोन में क्रोमियम ट्राइऑक्साइड (जोन्स अभिकर्मक, Jone’s regent) भी 2° ऐल्कोहॉल को ऐल्केनोन में बदल देता है।
इसी प्रकार 2° ऐल्कोहॉल Cu, 573K के साथ विहाइड्रोजनीकरण भी इसे ऐल्केनोन में परिवर्तित कर देता है।
साधारणतः ऐल्केनोन का ऑक्सीकरण कठिन है परन्तु प्रबल ऑक्सीकारक जैसे – Na2Cr2 O7 तथा सांद्र H2SO4 के साथ दीर्घकाल तक ऑक्सीकरण कराने पर ये ऑक्सीकृत होकर ऐल्केनाइक अम्लों का मिश्रण देते हैं। प्रत्येक अम्ल में मूल ऐल्केनोन की तुलना में कार्बन परमाणुओं की संख्या कम होती है।
ऐल्केनॉन का ऑक्सीकरण पोपॉफ के नियम (Propoff’s rule) के अनुसार होता है।
ऐल्केनोन के ऑक्सीकरण का पोपॉफ नियम –
ऐल्केनोन में कार्बोनिल समूह पर उपस्थित ऐल्किल समूहों के a- कार्बन परमाणुओं का ही ऑक्सीकरण होता है। कार्बोनिल समूह पर उपस्थित ऐल्किल समूह भिन्न हो तो प्रमुखतः उस ऐल्किल समूह के a-कार्बन परमाणु का ऑक्सीकरण होगा जिस पर हाइड्रोजन परमाणुओं की संख्या कम हो ।
यदि दोनों ऐल्किल समूहों में a- कार्बन परमाणु पर हाइड्रोजन परमाणुओं की संख्या समान हो तो कार्बोनिल समूह प्रमुखतः उस ऐल्किल समूह के साथ रहता है जिसमे कार्बन परमाणुओं की संख्या कम होती है।
(3) तृतीयक (3o) ऐल्कोहॉल का ऑक्सीकरण – तृतीयक ऐल्केहॉल का उदासीन अथवा क्षारीय विलयन में ऑक्सीकरण बहुत कठिन है परन्तु अम्लीय ऑक्सीकारकों से इनका शीघ्रता से ऑक्सीकरण हो जाता है। इनके ऑक्सीकरण पर ऐल्केनॉन और ऐल्केनोइक अम्ल का मिश्रण प्राप्त होता है जिनमें मूल ऐल्केनॉल की तुलना में कार्बन – परमाणुओं की संख्या कम होती है।
ऑक्सीकरण अभिक्रियाऐं भी प्राथमिक, द्वितीयक तथा तृतीयक ऐल्केनॉल में विभेद करने हेतु प्रयुक्त की जाती है।
(4) ऐल्केनॉल का ऑक्सीकरण H2O2 तथा FeSO4 (फेन्टन अभिकर्मक) द्वारा करने पर इनका द्विलकीकरण (Dimerisation) हो जाता है तथाडाइऑल प्राप्त होता है। जैसे 2- मेथिल – 2- प्रोपेनॉल से 2,5- डाइमेथिल हेक्सेन -2, 5- डाइऑल मिलता है।
(5) हैलोजन जलीय या क्षारीय विलयन में ऐल्कोहॉलों का कार्बोनिल यौगिकों में ऑक्सीकरण कर देते हैं। उदाहरणार्थ-
(i) जलीय माध्यम में-
स्वेन (Swain, 1961) के अनुसार जलीय विलयन में अभिक्रिया क्रियाविधि हाइड्राइड आयन के पृथक्करण से होती है।
क्षारकीय विलयन में अभिक्रिया निम्न प्रकार सम्पन्न होती है-
(6) विहाइड्रोजनीकरण (De hydrogenation ) – ऐल्केनॉल वाष्प को 573K ताप पर तप्त ताम्र पर प्रवाहित करने पर प्राथमिक, द्वितीयक और तृतीयक ऐल्केनॉल से क्रमशः ऐल्केनैल, ऐल्केनॉन और ऐल्कीन प्राप्त होती है। तृतीयक ऐल्केनॉल का विहाइड्रोजनीकरण न होकर इस स्थिति में निर्जलीकरण होता है।
(7) अकार्बनिक अम्लों से अभिक्रिया: ऐल्कोहॉल, अकार्बनिक अम्लों के साथ अभिक्रिया पर लवण बनाते हैं।
परन्तु उपरोक्त अभिक्रिया 150° पर कराते हैं तो ईथर प्राप्त होते हैं ।
(8) हैलोफार्म अभिक्रिया : वे ऐल्कोहॉल जिनमें समूह होता है, क्षार की उपस्थिति में हैलोजन से अभिक्रिया पर हैलोफार्म बनाते हैं। उदाहरणार्थ,
यदि अभिक्रिया आयोडीन तथा NaOH के साथ कराते हैं तो पीले रंग का आयडोफार्म बनता है।
प्राथमिक द्वितीयक एवं तृतीयक ऐल्कोहॉलों में विभेद (Distinction between Primary, Secondary and Tertiary alcohols)
(1) विक्टर मेयर परीक्षण (Victor Meyer’s test) :- ऐल्कोहॉल फास्फोरस तथा आयोडीन से अभिक्रिया पर ऐल्किल आयोडाइड बनाते हैं जो सिल्वर नाइट्राइट के साथ अभिक्रिया पर ऐल्किल नाइट्रेट देते हैं विभिन्न ऐल्कोहोलों के नाइट्राइटों का भिन्न-भिन्न व्यवहार होता है जिनके आधार पर विभिन्न ऐल्कोहॉलों की पहचान की जा सकती है ।
(i) प्राथमिक ऐल्कोहॉलों के नाइट्राइटों की अभिक्रिया नाइट्रस अम्ल में कराने पर नाइट्रोलिक अम्ल बनता है जो NaOH के साथ सोडियम नाइट्रोलेट देता है जिसका लाल रंग होता है।
(ii) द्वितीयक ऐल्कोहलों के नाइट्राइट, नाइट्रस अम्ल के साथ क्रिया पर छद्म नाइट्र जो प्रोटोन की अनुपस्थिति के कारण NaOH के साथ क्रिया नहीं करता है तथा किसी कार्बनि के साथ नीला रंग देता है।
हिंदी माध्यम नोट्स
Class 6
Hindi social science science maths English
Class 7
Hindi social science science maths English
Class 8
Hindi social science science maths English
Class 9
Hindi social science science Maths English
Class 10
Hindi Social science science Maths English
Class 11
Hindi sociology physics physical education maths english economics geography History
chemistry business studies biology accountancy political science
Class 12
Hindi physics physical education maths english economics
chemistry business studies biology accountancy Political science History sociology
English medium Notes
Class 6
Hindi social science science maths English
Class 7
Hindi social science science maths English
Class 8
Hindi social science science maths English
Class 9
Hindi social science science Maths English
Class 10
Hindi Social science science Maths English
Class 11
Hindi physics physical education maths entrepreneurship english economics
chemistry business studies biology accountancy
Class 12
Hindi physics physical education maths entrepreneurship english economics