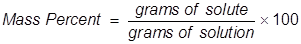विलयन की सांद्रता को व्यक्त करना , विलयन की सांद्रता का सूत्र , परिभाषा (concentration of solution in chemistry in hindi)
सांद्रता को निम्न प्रकार परिभाषित किया जा सकता है –
सान्द्रता की परिभाषा “विलेय की वह मात्रा जो विलयन या विलायक की एक निश्चित मात्रा या आयतन में घुली रहती है उसे विलयन की सांद्रता कहते है। ”
जब किसी विलयन में या विलायक में विलेय पदार्थ की मात्रा अधिक घुली रहती है तो हम कहते है कि इसकी सांद्रता अधिक है अर्थात विलेय की घुली हुई मात्रा को ही सान्द्रता कहते है।
विलयन की सांद्रता को निम्न प्रकार प्रदर्शित किया जाता है –
1. द्रव्यमान प्रतिशत (mass percentage %W/W)
2. आयतन प्रतिशत (volume percentage %v/v)
3. द्रव्यमान आयतन प्रतिशत (%W/V)
4. पार्ट्स प्रति मिलियन (parts per million)
5. मोल अंश या मोल भिन्न या मोल प्रभाज (mole fraction)
6. नॉर्मलता (normality)
7. मोलरता (Molarity)
8. फॉर्मलता (formality) (F)
9. मोललता (molality) (m)
अब हम इन सभी के बारे में विस्तार से अध्ययन करते है –
1. द्रव्यमान प्रतिशत (mass percentage %W/W)
2. आयतन प्रतिशत (volume percentage %v/v)
3. द्रव्यमान आयतन प्रतिशत (%W/V)
4. पार्ट्स प्रति मिलियन (parts per million)
5. मोल अंश या मोल भिन्न या मोल प्रभाज (mole fraction)
6. नॉर्मलता (normality) (N)
7. मोलरता (Molarity) (M)
8. फॉर्मलता (formality) (F)
9. मोललता (molality) (m)
हिंदी माध्यम नोट्स
Class 6
Hindi social science science maths English
Class 7
Hindi social science science maths English
Class 8
Hindi social science science maths English
Class 9
Hindi social science science Maths English
Class 10
Hindi Social science science Maths English
Class 11
Hindi sociology physics physical education maths english economics geography History
chemistry business studies biology accountancy political science
Class 12
Hindi physics physical education maths english economics
chemistry business studies biology accountancy Political science History sociology
English medium Notes
Class 6
Hindi social science science maths English
Class 7
Hindi social science science maths English
Class 8
Hindi social science science maths English
Class 9
Hindi social science science Maths English
Class 10
Hindi Social science science Maths English
Class 11
Hindi physics physical education maths entrepreneurship english economics
chemistry business studies biology accountancy
Class 12
Hindi physics physical education maths entrepreneurship english economics