1. अभिकारक की सान्द्रता : द्रव्य अनुपाती क्रिया नियम के अनुसार अभिक्रिया
वेग अभिकारको की
सांद्रता के समानुपाती होता है अर्थात अभिकारको की सांद्रता बढ़ने पर अभिक्रिया वेग बढ़ता है।
2. ताप का प्रभाव : सामान्यत:
ताप बढाने पर रासायनिक अभिक्रिया का वेग बढ़ता है क्योंकि ताप बढ़ाने से अभिकारक अणुओं की
गतिज ऊर्जा बढ़ने के कारण इनके मध्य टक्करों की संख्या बढती है और टक्करों की संख्या बढने से सक्रीय अणुओं की संख्या बढती है इसलिए अभिक्रिया वेग बढ़ जाता है।
प्रत्येक 10 डिग्री सेल्सियस ताप वृद्धि से अभिक्रिया का वेग लगभग 2 से 3 गुना बढ़ जाता है।
3. अभिकारको की प्रकृति : यह भी अभिक्रिया वेग को प्रभावित करती है क्योंकि अभिक्रिया के दौरान अभिकारक अणुओं के मध्य पुराने बंध टूटते है एवं नए बन्ध बनते है अत: यदि अभिकारक अणुओं की बंध सामर्थ्य कम हो तो बन्ध आसानी से वियोजित होगा , इसलिए अभिक्रिया वेग अधिक होगा।
जैसे : CO की तुलना में NO की बंध सामर्थ्य कम है अत:
2NO + O2 → 2NO2 (तीव्र गति से)
2CO + O2 → 2CO2 (मंद गति से)
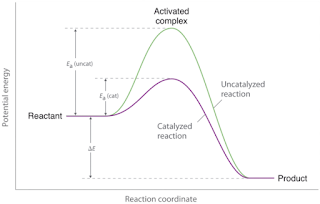
4. उत्प्रेरक का प्रभाव : सामान्यत: उत्प्रेरक की उपस्थिति में रासायनिक अभिक्रिया का वेग बढ़ जाता है क्योंकि उत्प्रेरक के कारण अभिक्रिया में सक्रियण ऊर्जा के मान में कमी आ जाती है।
उत्प्रेरक का सक्रियण ऊर्जा पर प्रभाव दर्शाने वाला वक्र निम्न प्रकार है –
5. अभिकारको की सतह का क्षेत्रफल : अभिकारको की सतह का क्षेत्रफल बढ़ने से अभिक्रिया का वेग बढ़ता है इसलिए अभिक्रिया में अभिकारको को महीन चूर्ण के रूप में लेते है।
जैसे : लकड़ी का एक बड़ा टुकड़ा धीमी गति से जलता है लेकिन यदि इसके छोटे छोटे टुकड़े कर दिया जाए तो सतह का क्षेत्रफल बढ़ने के कारण यह तीव्र गति से जलता है।
6. विकिरणों का प्रभाव : विकिरणों की उपस्थिति में अभिक्रिया का वेग बढ़ जाता है। जैसे : H2
व Cl2 के मध्य अभिक्रिया अंधेरे में मंद गति से होती है जबकि सूर्य के प्रकाश में तीव्र गति से होती है।
H2 + Cl2 → 2HCl
शून्य कोटि अभिक्रिया : ऐसी अभिक्रियाएँ जिनमे अभिक्रिया का वेग किसी भी अभिकारक
अणु की सांद्रता पर निर्भर नहीं करता शून्य कोटि अभिक्रिया कहलाती है।
या
ऐसी अभिक्रिया जिसमे अभिक्रिया का वेग अभिकारको की सान्द्रता के शून्य घात के समानुपाती हो , शून्य कोटि की अभिक्रिया कहलाती है।
शून्य कोटि अभिक्रिया की अवकलित व समाकलित वेग समीकरण (zero order reaction derivation) :
A → product (उत्पाद)
t = 0 समय पर a → 0
t समय पर (a-x) → x
अभिक्रिया वेग = -d[A]/dt = +dx/dt ∝ [A]0
∝ का चिन्ह हटाने पर –
dx/dt = K0[A]0
यदि [A]0 = 1 तो dx/dt = K0 (समीकरण 1)
समीकरण 1 शून्य कोटि की अभिक्रिया की अवकलित वेग समीकरण है।
समीकरण 1 से –
dx = K0 dt
समाकलन करने पर –
x = K0t + C (समीकरण 2)
c = समाकलन स्थिरांक है इसका मान प्राप्त करने के लिए प्रारंभिक दशाएं आरोपित करने पर
t = 0 समय पर x = 0
अत: c = 0 होगा।
c = 0 समीकरण-2 में रखने पर
x = K0 t (समीकरण-3)
K0 = x/t (समीकरण-4)
अत: समीकरण-4 शून्य कोटि अभिक्रिया की समाकलित समीकरण है।
अर्द्ध आयु (t1/2) : अर्द्धआयु वह समय होता है जब अभिक्रिया में अभिकारको की सान्द्रता अपनी प्रारंभिक सांद्रता की आधी रह जाती है।
समीकरण-4 से
K0 = x/t से
t = x/K0
माना अभिकारक की प्रारंभिक सांद्रता = a मोल/लीटर है तो t1/2 समय में इसकी सांद्रता a/2 मोल/लीटर होगी तथा उत्पाद की सान्द्रता (x) = a/2 होगी।
अत: उपरोक्त समीकरण में t = t1/2 व x = a/2 रखने पर :-
t1/2 = a/2K0 (समीकरण-5)
समीकरण-5 से शून्य कोटि अभिक्रिया की अर्द्ध आयु ज्ञात कर सकते है तथा इस समीकरण से स्पष्ट है कि शून्य कोटि अभिक्रिया की अर्द्धआयु , अभिकारक की सांद्रता पर निर्भर करता है।
अर्थात t1/2 ∝ a
वेग स्थिरांक की इकाई = [Mol1L-1 S-1]
शून्य कोटि अभिक्रिया के उदाहरण :
1. जल की सतह पर सूर्य के
प्रकाश की उपस्थिति में
H2 व Cl2 के मध्य होने वाली अभिक्रिया शून्य कोटि की होती है।
H2 + Cl2 → 2HCl
अभिक्रिया वेग = K0[H2]0[Cl2]0
2. धातु उत्प्रेरक की सतह पर होने वाली अभिक्रियाएँ शून्य कोटि की होती है।
उदाहरण : PH3 का विघटन :
2PH3 → 2P + 3H2 (MO और उच्च दाब की उपस्थिति)